Il trattamento dell’ictus acuto nella medicina personalizzata – L’impatto di un meteorite nel cervello
Un coagulo di sangue nel cervello che blocca l’apporto di ossigeno può causare un ictus acuto ed in questi casi, ogni minuto è importante. Un team dell’Empa, dell’Ospedale Universitario di Ginevra e della Clinica Hirslanden sta attualmente sviluppando una procedura diagnostica che può essere utilizzata per iniziare tempestivamente una terapia su misura, come riportato nell’attuale numero della rivista scientifica “Scientific Reports”.
Non ci sono segnali di allarme: Da un momento all’altro, intere aree cerebrali vengono bloccate. Quando un coagulo occlude un vaso sanguigno, l’apporto di ossigeno al cervello viene interrotto e la persona colpita subisce un ictus cerebrale acuto. Questa condizione pericolosa per la vita può manifestarsi in molti modi diversi: dalla paralisi muscolare alla perdita dell’udito o della vista, fino alla perdita di coscienza. Ma una cosa è certa: Si tratta di un’emergenza medica e il tempo necessario per risolvere l’ostruzione vascolare deve essere il più breve possibile per salvare il maggior numero possibile di cellule nervose dalla morte. Questo è l’unico modo per prevenire danni neurologici permanenti.
Quale sia il trattamento più adatto a questo scopo non è sempre facile da determinare con la necessaria rapidità. Sulla base dell’analisi a raggi X e della microscopia elettronica, un team dell’Empa, della Clinica Hirslanden e dell’Ospedale Universitario di Ginevra sta attualmente sviluppando un metodo che dovrebbe consentire di individuare la terapia ottimale nel più breve tempo possibile. Un primo studio è stato pubblicato sulla rivista scientifica Scientific Reports. Questi dati dovrebbero costituire la base per un trattamento su misura nel senso della medicina personalizzata.
Organi rigenerati, medicina spaziale e sanità senza barriere
Esaminare ogni cellula individualmente
Il motivo di questo dilemma: non tutti i coaguli di sangue sono uguali; a seconda del tipo, possono aggregarsi diversi tipi di cellule. A seconda della predominanza di globuli rossi o bianchi, o della percentuale di fibre di fibrina, il trombo ha proprietà completamente diverse. Inoltre, i trombi differiscono notevolmente nella forma. Un trombo lungo 15 millimetri che non riempie completamente un vaso sanguigno ha proprietà meccaniche diverse rispetto a un coagulo di pochi millimetri che blocca completamente un vaso e l’afflusso di sangue alle aree cerebrali retrostanti. Il trattamento ottimale dipende da queste differenze, sia che si tratti di sciogliere il coagulo con farmaci o di utilizzare un cosiddetto stent retriever, una sorta di piccola canna da pesca con cui è possibile “ripescare” il trombo nel vaso sanguigno e il cui materiale può essere selezionato in modo diverso a seconda del trombo.
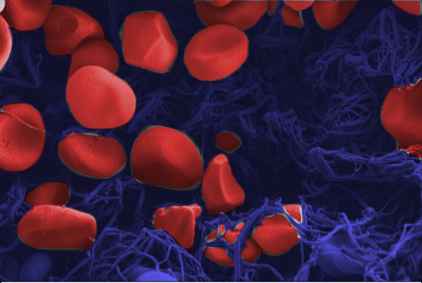
Attualmente la radiologia si basa su scansioni convenzionali di tomografia computerizzata per prendere una decisione terapeutica. Tuttavia, le immagini della testa del paziente forniscono poche informazioni sui dettagli di un coagulo perché gli oggetti fatti di materiali simili sono troppo difficili da distinguere l’uno dall’altro e da risolvere spazialmente. Inoltre, nella pratica clinica quotidiana la risoluzione delle immagini è limitata a 200 micrometri.
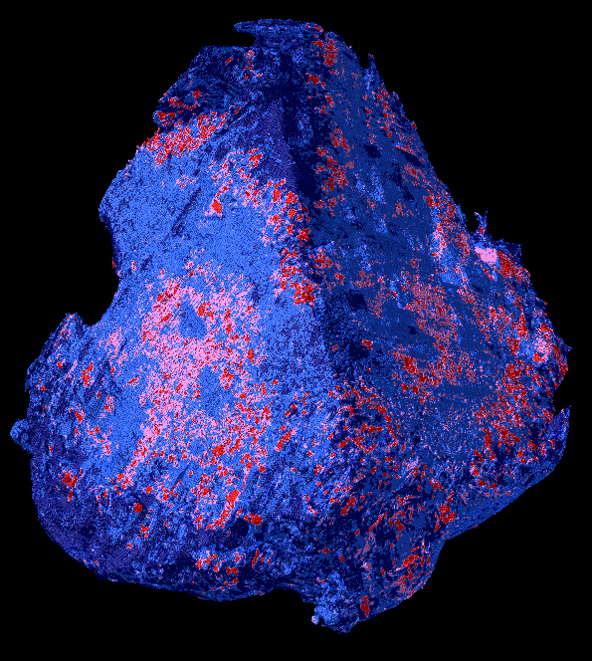
La situazione è diversa con i metodi di laboratorio, che i ricercatori hanno utilizzato per il loro nuovo studio: Il team, con la partecipazione di Robert Zboray, Antonia Neels e Somayeh Saghamanesh del Center for X-Ray Analytics dell’Empa, ha esaminato diversi coaguli di sangue prelevati da pazienti durante interventi neurochirurgici. A questo scopo, sono state combinate diverse tecnologie di laboratorio, ottenendo immagini virtuali in 3D che hanno rivelato proprietà dettagliate e precedentemente sconosciute dei coaguli di sangue. “Abbiamo utilizzato la micro-tomografia 3D per esaminare i singoli globuli rossi fino alla gamma dei micrometri“, spiega Zboray, ricercatore dell’Empa. La tomografia che utilizza tecniche a contrasto di fase produce un contrasto più forte. Gli oggetti facili da penetrare, come i muscoli, il tessuto connettivo o i coaguli di sangue, possono così essere visualizzati in sfumature particolarmente fini e nella loro diffusione spaziale.
Trombi calcificati
Altre tecnologie, come la microscopia elettronica a scansione e i metodi di diffrazione e diffusione dei raggi X, hanno fornito ulteriori informazioni fino a livelli atomici. In questo caso è stato dimostrato per la prima volta che un trombo non è costituito solo da cellule ematiche e reti di fibrina, ma può anche essere inframmezzato da minerali come l’idrossiapatite, come è noto dalle pareti dei vasi nella calcificazione arteriosa.
Tuttavia, queste informazioni dettagliate sulle peculiarità di un coagulo di sangue arrivano troppo tardi, quando il trombo è già stato rimosso chirurgicamente. Inoltre, i nuovi dati acquisiti non possono essere confrontati con le immagini e i risultati convenzionali dell’ospedale. La digitalizzazione in medicina, invece, consente di modellare i dati in modo tale che un algoritmo possa leggere le informazioni dettagliate in futuro. “Per fare questo, dobbiamo ancora studiare un gran numero di trombi in modo da poter utilizzare l’apprendimento automatico per identificare nuove caratteristiche e modelli di immagine relativi alla composizione del coagulo, che possono poi essere trasferiti alle immagini ospedaliere convenzionali per aiutare a distinguere i diversi tipi di trombi“, ha detto Zboray.
Alla fine, i ricercatori sperano che, grazie alle loro scoperte, le immagini ospedaliere convenzionali possano essere interpretate in un tempo molto breve, proprio come se il coagulo di sangue fosse stato esaminato in un laboratorio virtuale ultraveloce. Questo aprirebbe la strada a una terapia più accurata e personalizzata per i pazienti colpiti da ictus in modo tempestivo.
Fonte: Federal Laboratory for Materials Testing and Research http://www.empa.ch





